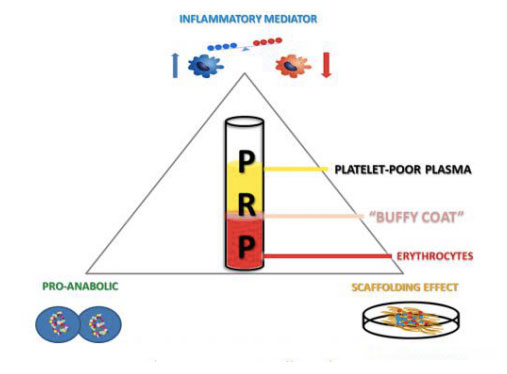
Jēdziens, kas mūsdienās pazīstams kā PRP, pirmo reizi parādījās hematoloģijas jomā 1970. gados.Hematologi terminu PRP ieviesa pirms gadu desmitiem, mēģinot aprakstīt plazmu, kas iegūta no trombocītu skaita, kas pārsniedz bazālo vērtību perifērajās asinīs.Vairāk nekā desmit gadus vēlāk PRP tika izmantots sejas žokļu ķirurģijā kā trombocītiem bagāta fibrīna (PRF) forma.Fibrīna saturs šajā PRP atvasinājumā ir ļoti vērtīgs tā adhezīvo un homeostatisko īpašību dēļ, savukārt PRP piemīt noturīgas pretiekaisuma īpašības un tas stimulē šūnu proliferāciju.Visbeidzot, aptuveni deviņdesmitajos gados PRP kļuva populārs, un galu galā tehnoloģija tika pārnesta uz citām medicīnas jomām.Kopš tā laika šī pozitīvā bioloģija ir plaši pētīta un izmantota dažādu balsta un kustību aparāta traumu ārstēšanā profesionāliem sportistiem, vēl vairāk veicinot tās plašo mediju uzmanību.Papildus tam, ka PRP ir efektīvs ortopēdijā un sporta medicīnā, to izmanto oftalmoloģijā, ginekoloģijā, uroloģijā un kardioloģijā, pediatrijā un plastiskajā ķirurģijā.Pēdējos gados PRP ir atzinīgi novērtējuši arī dermatologi par tā iespējām ārstēt ādas čūlas, rētu pārskatīšanu, audu reģenerāciju, ādas atjaunošanos un pat matu izkrišanu.
Ņemot vērā faktu, ka ir zināms, ka PRP tieši manipulē ar dziedināšanas un iekaisuma procesiem, kā atsauce ir jāievieš dziedināšanas kaskāde.Dziedināšanas process ir sadalīts šādos četros posmos: hemostāze;iekaisums;šūnu un matricas proliferācija un visbeidzot brūču remodelēšana.
1. Audu dziedināšana
Tiek aktivizēta audu dziedināšanas kaskāde — process, kas izraisa trombocītu agregāciju, trombu veidošanos un īslaicīgas ārpusšūnu matricas veidošanos (ECM. Pēc tam trombocīti pielīp pie eksponētiem kolagēna un ECM proteīniem, izraisot α-granulu klātbūtni izdalīšanās procesā). Bioaktīvās molekulas.Trombocīti satur dažādas bioaktīvas molekulas, tostarp augšanas faktorus, ķīmokīnus un citokīnus, kā arī pro-iekaisuma mediatorus, piemēram, prostaglandīnus, prostatas ciklīnu, histamīnu, tromboksānu, serotonīnu un bradikinīnu.
Dziedināšanas procesa pēdējais posms ir atkarīgs no brūces pārveidošanas.Audu remodelēšana ir stingri regulēta, lai izveidotu līdzsvaru starp anaboliskajām un kataboliskajām reakcijām.Šajā fāzē trombocītu izcelsmes augšanas faktors (PDGF), transformējošais augšanas faktors (TGF-β) un fibronektīns stimulē fibroblastu proliferāciju un migrāciju, kā arī ECM komponentu sintēzi.Tomēr brūces nobriešanas laiks lielā mērā ir atkarīgs no brūces smaguma pakāpes, individuālajām īpašībām un ievainoto audu specifiskās dziedināšanas spējas, un daži patofizioloģiski un vielmaiņas faktori var ietekmēt dzīšanas procesu, piemēram, audu išēmija, hipoksija, infekcija. , augšanas faktora nelīdzsvarotība un pat ar vielmaiņas sindromu saistītas slimības.
Iekaisuma veicinoša mikrovide, kas traucē dzīšanas procesu.Lai sarežģītu situāciju, ir arī augsta proteāzes aktivitāte, kas kavē augšanas faktora (GF) dabisko darbību.Papildus mitogēnām, angiogēnām un ķīmijtaktiskām īpašībām PRP ir arī bagātīgs daudzu augšanas faktoru, biomolekulu avots, kas var neitralizēt kaitīgo ietekmi iekaisušos audos, kontrolējot saasinātu iekaisumu un radot anaboliskus stimulus.Ņemot vērā šīs īpašības, pētnieki var atrast lielu potenciālu dažādu sarežģītu traumu ārstēšanā.
2. Citokīns
Citokīniem PRP ir galvenā loma audu atjaunošanas procesu manipulācijās un iekaisuma bojājumu regulēšanā.Pretiekaisuma citokīni ir plašs bioķīmisko molekulu spektrs, kas mediē pro-iekaisuma citokīnu reakcijas, ko galvenokārt izraisa aktivēti makrofāgi.Pretiekaisuma citokīni mijiedarbojas ar specifiskiem citokīnu inhibitoriem un šķīstošiem citokīnu receptoriem, lai modulētu iekaisumu.Interleikīna (IL)-1 receptoru antagonisti IL-4, IL-10, IL-11 un IL-13 ir klasificēti kā galvenie pretiekaisuma citokīni.Atkarībā no brūces veida dažiem citokīniem, piemēram, interferonam, leikēmijas inhibējošajam faktoram, TGF-β un IL-6, var būt pretiekaisuma vai pretiekaisuma iedarbība.TNF-α, IL1 un IL-18 ir noteikti citokīnu receptori, kas var kavēt citu proteīnu pro-iekaisuma iedarbību [37].IL-10 ir viens no spēcīgākajiem pretiekaisuma citokīniem, tas var samazināt pro-iekaisuma citokīnus, piemēram, IL-1, IL-6 un TNF-α, un paaugstināt pretiekaisuma citokīnu darbību.Šiem pretregulācijas mehānismiem ir būtiska loma iekaisuma veicinošo citokīnu ražošanā un darbībā.Turklāt daži citokīni var izraisīt specifiskas signalizācijas reakcijas, kas stimulē fibroblastus, kas ir būtiski audu atjaunošanai.Iekaisuma citokīni TGFβ1, IL-1β, IL-6, IL-13 un IL-33 stimulē fibroblastus diferencēties miofibroblastos un uzlabo ECM [38].Savukārt fibroblasti izdala citokīnus TGF-β, IL-1β, IL-33, CXC un CC ķemokīnus, kas veicina pro-iekaisuma reakcijas, aktivizējot un piesaistot imūnās šūnas, piemēram, makrofāgus.Šīm iekaisuma šūnām ir vairākas lomas brūces vietā, galvenokārt veicinot brūces klīrensu, kā arī ķemokīnu, metabolītu un augšanas faktoru biosintēzi, kas ir būtiski jaunu audu pārveidošanai.Tādējādi PRP esošajiem citokīniem ir svarīga loma šūnu tipa mediētas imūnās atbildes stimulēšanā, veicinot iekaisuma fāzes izzušanu.Faktiski daži pētnieki ir nosaukuši šo procesu par "reģeneratīvo iekaisumu", kas liecina, ka iekaisuma fāze, neskatoties uz pacienta satraukumu, ir kritisks solis, kas nepieciešams, lai audu atjaunošanas process nonāktu veiksmīgā noslēgumā, ņemot vērā epiģenētiskos mehānismus, ar kuriem iekaisuma signāli veicina šūnu darbību. plastiskums.
3. Fibrīns
Trombocīti satur vairākus ar fibrinolītisko sistēmu saistītus faktorus, kas var pastiprināt vai pazemināt fibrinolītisko reakciju.Hematoloģisko komponentu un trombocītu funkcijas laika attiecības un relatīvais ieguldījums trombu degradācijā joprojām ir jautājums, par kuru sabiedrībā ir vērts diskutēt.Literatūrā ir sniegti daudzi pētījumi, kas koncentrējas tikai uz trombocītiem, kas ir pazīstami ar savu spēju ietekmēt dzīšanas procesu.Neskatoties uz daudziem izciliem pētījumiem, ir konstatēts, ka arī citi hematoloģiskie komponenti, piemēram, koagulācijas faktori un fibrinolītiskā sistēma, būtiski veicina efektīvu brūču atjaunošanos.Pēc definīcijas fibrinolīze ir sarežģīts bioloģisks process, kas balstās uz noteiktu enzīmu aktivāciju, lai veicinātu fibrīna noārdīšanos.Citi autori ir ierosinājuši fibrinolītisko reakciju, ka fibrīna noārdīšanās produkti (fdp) faktiski var būt molekulāri aģenti, kas ir atbildīgi par audu remonta stimulēšanu, svarīgu bioloģisku notikumu secību pirms fibrīna nogulsnēšanās un izņemšanu no angioģenēzes, kas ir nepieciešama brūču dzīšanai .Trombu veidošanās pēc traumas darbojas kā aizsargslānis, kas aizsargā audus no asins zuduma, mikrobu aģentu invāzijas, kā arī nodrošina pagaidu matricu, caur kuru šūnas var migrēt remonta laikā.Trombs rodas fibrinogēna šķelšanās dēļ, ko veic serīna proteāzes, un trombocīti agregējas šķērssaistītajā fibrīna šķiedru tīklā.Šī reakcija ierosina fibrīna monomēru polimerizāciju, kas ir galvenais asins recekļu veidošanās notikums.Trombi var darboties arī kā rezervuāri citokīniem un augšanas faktoriem, kas izdalās pēc aktivēto trombocītu degranulācijas.Fibrinolītisko sistēmu stingri regulē plazmīns, un tai ir galvenā loma šūnu migrācijas veicināšanā, augšanas faktora biopieejamības veicināšanā un citu audu iekaisumā un reģenerācijā iesaistīto proteāzes sistēmu regulēšanā.Ir zināms, ka fibrinolīzes galvenie komponenti, piemēram, urokināzes plazminogēna aktivatora receptors (uPAR) un plazminogēna aktivatora inhibitors-1 (PAI-1), tiek ekspresēti mezenhimālajās cilmes šūnās (MSC), kas ir specializēts šūnu tips, kas nepieciešams veiksmīgai brūču dzīšanai.
4. Šūnu migrācija
Plazmogēna aktivizēšana, izmantojot uPA-uPAR asociāciju, ir process, kas veicina iekaisuma šūnu migrāciju, jo tas uzlabo ekstracelulāro proteolīzi.Tā kā uPAR nav transmembrānu un intracelulāru domēnu, olbaltumvielai ir nepieciešami līdzreceptori, piemēram, integrīni un vitreīni, lai regulētu šūnu migrāciju.Turklāt uPA-uPAR saistīšanās palielināja uPAR afinitāti pret stiklveida konneksīniem un integrīniem, veicinot šūnu adhēziju.Plazminogēna aktivatora inhibitors-1 (PAI-1) savukārt atvieno šūnas, iznīcinot upar-vitreīnu un integrīnu, kad tas saistās ar uPA-upar-integrīna kompleksa uPA uz šūnas virsmas Stikla vokseļu mijiedarbība.
Reģeneratīvās medicīnas kontekstā mezenhimālās cilmes šūnas tiek mobilizētas no kaulu smadzenēm smagu orgānu bojājumu kontekstā, un tādējādi tās var atrast pacientu ar vairākiem lūzumiem asinsritē.Tomēr noteiktos apstākļos, piemēram, beigu stadijas nieru mazspēja, beigu stadijas aknu mazspēja vai atgrūšanas sākumā pēc sirds transplantācijas, šīs šūnas var nebūt nosakāmas asinīs [66].Interesanti, ka šīs cilvēka kaulu smadzenēs iegūtās mezenhimālās (stromas) cilmes šūnas nevar noteikt veselu indivīdu asinīs [67].Iepriekš tika ierosināta arī uPAR loma kaulu smadzeņu mezenhimālo cilmes šūnu mobilizēšanā, līdzīgi tam, kas notiek hematopoētisko cilmes šūnu (HSC) mobilizēšanā.Varabaneni et al.Rezultāti parādīja, ka granulocītu koloniju stimulējošā faktora izmantošana pelēm ar uPAR deficītu izraisīja MSC neveiksmi, vēlreiz pastiprinot fibrinolītiskās sistēmas atbalstošo lomu šūnu migrācijā.Turpmākie pētījumi ir arī parādījuši, ka glikozilfosfatidilinozīta enkurotie uPA receptori regulē adhēziju, migrāciju, proliferāciju un diferenciāciju, aktivizējot noteiktus intracelulāros signālu ceļus, šādi: izdzīvošanas fosfatidilinozīta 4,5-bisfosfāta 3-kināzes ceļi/Ak2 un ERK1/Ak2. un adhēzijas kināzi (FAK).
MSC ir pierādījuši papildu nozīmi brūču dzīšanas kontekstā.Piemēram, pelēm ar plazminogēna deficītu brūču dzīšanas notikumi ievērojami aizkavējās, kas liecina, ka plazmīns ir kritiski iesaistīts šajā procesā.Cilvēkiem plazmīna zudums var izraisīt arī brūču dzīšanas komplikācijas.Asins plūsmas traucējumi var ievērojami kavēt audu reģenerāciju, kas izskaidro, kāpēc šie reģeneratīvie procesi ir grūtāki diabēta pacientiem.
5. Monocīti un reģenerācijas sistēmas
Saskaņā ar literatūru, ir daudz diskusiju par monocītu lomu brūču dzīšanas procesā.Makrofāgi galvenokārt ir iegūti no asins monocītiem, un tiem ir svarīga loma reģeneratīvajā medicīnā [81].Tā kā neitrofīli izdala IL-4, IL-1, IL-6 un TNF-α, šīs šūnas parasti iekļūst brūces vietā aptuveni 24–48 stundas pēc traumas.Trombocīti atbrīvo trombīnu un trombocītu faktoru 4 (PF4), divus ķīmokīnus, kas veicina monocītu piesaisti un to diferenciāciju makrofāgos un dendritiskajās šūnās.Pārsteidzoša makrofāgu iezīme ir to plastiskums, ti, to spēja pārslēgt fenotipus un transdiferencēties citos šūnu veidos, piemēram, endotēlija šūnās, kas pēc tam parāda dažādas funkcijas, reaģējot uz dažādiem bioķīmiskiem stimuliem brūces mikrovidē.Iekaisuma šūnas izsaka divus galvenos fenotipus, M1 vai M2, atkarībā no vietējā molekulārā signāla, kas ir stimula avots.M1 makrofāgus inducē mikrobu aģenti, un tādējādi tiem ir lielāka pretiekaisuma iedarbība.Turpretim M2 makrofāgus parasti rada 2. tipa reakcija, un tiem ir pretiekaisuma īpašības, ko parasti raksturo IL-4, IL-5, IL-9 un IL-13 palielināšanās.Tas ir iesaistīts arī audu atjaunošanā, veidojot augšanas faktorus.Pāreju no M1 uz M2 izoformām lielā mērā nosaka vēlākie brūču dzīšanas posmi, kur M1 makrofāgi izraisa neitrofilu apoptozi un ierosina šo šūnu klīrensu).Neitrofilu izraisītā fagocitoze aktivizē notikumu ķēdi, kurā tiek izslēgta citokīnu ražošana, polarizējot makrofāgus un atbrīvojot TGF-β1.Šis augšanas faktors ir galvenais miofibroblastu diferenciācijas un brūču kontrakcijas regulators, kas ļauj novērst iekaisumu un uzsākt proliferācijas fāzi dziedināšanas kaskādē [57].Vēl viens ļoti saistīts proteīns, kas iesaistīts šūnu procesos, ir serīns (SG).Ir konstatēts, ka šis hematopoētisko šūnu izdalītais granulāts ir nepieciešams izdalīto proteīnu uzglabāšanai specifiskās imūnās šūnās, piemēram, tuklo šūnās, neitrofilos un citotoksiskajos T limfocītos.Lai gan daudzas ne-hematopoētiskās šūnas arī sintezē serotonīnu, visas iekaisuma šūnas ražo lielu daudzumu šī proteīna un uzglabā to granulās turpmākai mijiedarbībai ar citiem iekaisuma mediatoriem, tostarp proteāzēm, citokīniem, ķīmokīniem un augšanas faktoru.Šķiet, ka negatīvi lādētas glikozaminoglikāna (GAG) ķēdes SG ir kritiskas sekrēcijas granulu homeostāzei, jo tās var saistīties ar būtiski uzlādētu granulu komponentu uzglabāšanu un atvieglot to uzglabāšanu šūnām, olbaltumvielām un GAG ķēdēm raksturīgā veidā.Attiecībā uz viņu iesaistīšanos PRP, Woulfe un kolēģi iepriekš ir parādījuši, ka SG deficīts ir cieši saistīts ar mainītu trombocītu morfoloģiju;trombocītu faktora 4, beta-tromglobulīna un PDGF uzglabāšanas defekti trombocītos;slikta trombocītu agregācija un sekrēcija in vitro un trombozes in vivo formas defekti.Tāpēc pētnieki secināja, ka šis proteoglikāns, šķiet, ir galvenais trombozes regulators.
Ar trombocītiem bagātus produktus var iegūt, savācot un centrifugējot cilvēka asinis, sadalot maisījumu dažādos slāņos, kas satur plazmu, trombocītus, leikocītus un leikocītus.Ja trombocītu koncentrācija ir augstāka par bazālajām vērtībām, kaulu un mīksto audu augšanu var paātrināt ar minimālām blakusparādībām.Autologo PRP produktu pielietošana ir salīdzinoši jauna biotehnoloģija, kas turpina uzrādīt daudzsološus rezultātus dažādu audu traumu stimulēšanā un uzlabošanā.Šīs alternatīvās terapeitiskās pieejas efektivitāti var saistīt ar plašu augšanas faktoru un proteīnu lokālu ievadīšanu, atdarinot un atbalstot fizioloģisko brūču dzīšanas un audu atjaunošanas procesus.Turklāt fibrinolītiskā sistēma nepārprotami būtiski ietekmē kopējo audu atjaunošanos.Papildus spējai mainīt iekaisuma šūnu un mezenhimālo cilmes šūnu piesaisti šūnās, tas modulē proteolītisko aktivitāti brūču dzīšanas zonās un mezodermālo audu, tostarp kaulu, skrimšļu un muskuļu, reģenerācijas laikā, un tāpēc tas ir galvenais muskuļu un skeleta medicīnas komponents.
Dziedināšanas paātrināšana ir daudzu medicīnas jomas profesionāļu ļoti pieprasīts mērķis, un PRP ir pozitīvs bioloģisks instruments, kas turpina piedāvāt daudzsološus sasniegumus stimulācijā un labi koordinētā reģeneratīvo notikumu tandēmā.Tomēr, tā kā šis terapeitiskais instruments joprojām ir sarežģīts, jo īpaši tāpēc, ka tas atbrīvo neskaitāmus bioaktīvus faktorus un to dažādos mijiedarbības mehānismus un signalizācijas efektus, ir nepieciešami turpmāki pētījumi.
(Šī raksta saturs tiek atkārtoti izdrukāts, un mēs nesniedzam nekādas tiešas vai netiešas garantijas par šajā rakstā ietvertā satura precizitāti, uzticamību vai pilnīgumu, un mēs neesam atbildīgi par šī raksta viedokļiem, lūdzu, saprotiet.)
Izlikšanas laiks: 19. jūlijs 2022